생명과학과 김찬혁 교수, 정원석 교수 공동연구팀 : Anti-inflammatory clearance of amyloid beta by a chimeric Gas6 fusion protein - 「Nature Medicine」
우리 학교 생명과학과 정현철, 이세영 박사과정 그리고 김찬혁, 정원석 교수 공동연구팀이 지난달 22일 기존의 심각한 염증 부작용을 없앤 새로운 형태의 알츠하이머병 치료제를 개발했다고 밝혔다. 새로운 치료제는 세포 포식작용에 관여하는 Gas6 단백질을 이용해 제작된 것으로, 기존의 항체 기반 치료제가 갖는 심각한 염증 부작용을 예방하는 한편 손상된 인지기능까지 향상할 수 있다는 점에서 큰 의의가 있다.
기존 알츠하이머병 치료제의 한계
알츠하이머병은 치매를 일으키는 가장 흔한 원인 질환이다. 기억력과 인지능력을 저하시키고, 심할 경우 사망에까지 이르게 하는 이 질환은 뇌에 축적된 아밀로이드 베타 응집체에 의해 발병한다는 것이 학계의 정설이다. 최근 특정 아밀로이드 베타 올리고머의 독성을 보고했던 논문이 조작되었다는 기사가 언론에 과장되어 보도되면서 이 사실에 대한 오해를 불러일으키기도 했지만, 비정상적으로 잘린 36~43개의 아미노산 조각들의 응집체가 알츠하이머병의 원인이라는 점은 의심할 여지가 없다.
알츠하이머병을 치료하는 가장 직접적인 방법은 뇌 속에 축적된 아밀로이드 베타 응집체를 제거하는 것이다. 기존에는 항체를 이용해 응집체를 제거하는 방식이 주를 이뤄왔다. 최근 아밀로이드 베타를 표적으로 하는 항체 기반 치료제인 아두헬름이 최초로 미국 FDA에서 알츠하이머병의 치료제로 승인되기도 했으나, 부작용에 관한 논란이 끊이지 않고 있다. 항체 기반 치료제를 처방받은 환자들에게서 나타나는 대표적인 부작용은 뇌 염증과 밀접한 관련이 있는 미세혈관 출혈이다. 포식작용을 통해 아밀로이드 베타를 제거하는 면역세포들은 표면에 Fc 수용체를 발현하는데, 항체 기반 치료제가 이 수용체를 통해 염증 반응을 일으키기 때문이다. 그뿐만 아니라, 항체 기반 치료제를 사용하면 환자의 인지 기능이 회복되지 않는다는 한계가 있었다. 따라서 기존의 심각한 염증 부작용을 해결하면서 아밀로이드 베타를 효과적으로 제거하는 치료제를 개발하는 일은 오랜 숙원이었다.
Gas6 융합단백질을 이용한 알츠하이머병 치료제
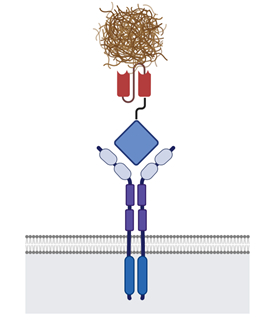
연구팀은 몸속에서 죽은 세포들을 제거하는 과정에 관여하는 Gas6 단백질에 주목했다. Gas6 단백질은 대식세포의 식세포작용을 매개하는 역할을 하는데, 단백질의 한쪽은 죽은 세포에 결합하고, 다른 쪽은 대식세포의 표면에서 발현되는 TAM 수용체에 결합한다. 연구팀은 단백질을 인위적으로 조작해 Gas6 단백질이 죽은 세포 대신 아밀로이드 베타에 결합하게 했다. 이렇게 만들어진 Gas6 융합단백질은 실험을 통해 뇌 안에서 아밀로이드 베타를 선택적으로 제거함과 동시에 염증반응을 억제함이 증명되었다.
연구팀은 알츠하이머 질병 쥐 모델을 통해 개발한 융합단백질이 뇌에서 식세포작용을 담당하는 미세아교세포와 별아교세포를 동시에 활용해 아밀로이드 베타의 양을 현저히 감소시킴을 확인했다. 기존의 항체 기반 치료제는 미세아교세포를 통해서만 아밀로이드 베타의 양을 줄일 수 있었다. 따라서 Gas6 융합단백질이 아밀로이드 베타를 제거하는 기전은 기존 치료제와 비교했을 때 뚜렷한 이점이 될 것으로 보인다. 항체 치료제를 투여한 알츠하이머 질병 쥐 모델에서는 미세아교세포에 의해 과도한 시냅스 제거 현상이 일어났지만, Gas6 융합단백질을 주입한 알츠하이머 질병 쥐 모델에서는 손상된 인지능력과 기억력이 항체 치료제보다 높은 수준으로 회복되었다는 점도 주목할 만하다. 더불어 항체 기반 치료제를 사용했을 때 나타나는 대표적인 부작용인 뇌 미세혈관 출혈도 현저하게 감소하여 새로운 기전의 단백질 치료제의 가능성을 시사한다.
Gas6 융합단백질의 활용 가능성
이번 연구를 통해 개발한 Gas6 융합단백질은 이전까지는 없던 새로운 작용기전을 가진 알츠하이머병 치료제로써, 다양한 퇴행성 뇌 질환과 자가 면역질환에 적용할 수 있을 것으로 기대된다. 현재 연구팀은 Gas6 융합단백질을 이용한 치료제를 상용화하기 위해 개발 과정을 거치고 있으며, 알츠하이머병을 유발하는 또 다른 원인으로 지목되는 타우 단백질을 표적으로 하는 치료제 개발도 계획하고 있다.
마지막으로 김 교수는 우리 학교 구성원들이 스스로 자부심을 가지고 하고 싶은 일에 매진하다 보면 원하는 목표를 이룰 수 있을 것이라며 독려했다. 정 교수는 교내 구성원들에게 생명 현상의 핵심적인 메커니즘을 밝혀내거나, 메커니즘에 기반하여 신약을 개발하는 등 다양한 분야의 연구가 이루어지고 있는 생명과학과에 많은 관심을 가져줄 것을 부탁하기도 했다.

