[생명과학과 김은준 교수팀] 생크2 유전자 결손으로 신호전달 감소, mGluR5 자극하면 치료 가능
우리 학교 생명과학과 김은준 교수팀이 서울대학교 강봉균 교수팀, 연세대학교 이민구 교수팀과 함께 자폐증 발병원인을 규명하고 치료법을 제시했다. 이 연구결과는 중요성을 인정받아 저명한 학술지 <네이처> 6월 14일 자와 자매지 <Nature Reviews Drug Discovery> 7월호에 연달아 게재되었다.
원인과 치료법, 검증된 것은 얼마 없어
최근 세계적으로 자폐증 환자가 증가하고 있다. 자폐증 환자는 사회성 결핍증상, 언어 소통 장애, 반복적인 행동을 하거나 관심을 특정 분야에만 제한적으로 나타내는 증상을 보인다. 현재 미국식약청 허가를 받은 자폐증 치료약 리스페리돈(Risperidone)은 세 번째 증상만을 완화하는 데에 효과가 있다. 첫 번째와 두 번째 증상을 회복시키는 치료법은 개발되어 있지 않았다.
자폐증은 원인도 제대로 규명되어 있지 않다. 자폐증 환자와 정상인의 유전자를 비교해본 결과, 자폐증의 발병원인으로 의심받고 있는 유전자는 수십 종에 이른다. 그러나 이 중 동물실험을 거쳐 검증된 것은 십여 종에 불과하다.
생크2 유전자가 자폐증 유발
재작년 <네이처 지네틱스>에 자폐증 환자들은 생크2(Shank2)라는 유전자에 이상이 있다는 관찰결과가 보고되었다. 김 교수팀과 이 교수팀은 실험 생쥐의 생크2를 인위적으로 결손 시키고 정상 생쥐들과 행동을 비교했다. 그 결과 생크2가 결손된 생쥐가 자폐증의 첫 번째 증상과 유사한 증상을 보인다는 것을 알아냈다. 이를 통해 생크2가 자폐증의 원인이 되는 유전자라는 것을 확인할 수 있었다.
자폐증 원인 메커니즘도 일부 규명해
김 교수팀은 자폐증 원인 메커니즘도 밝혀냈다. 생크2는 시냅스 단백질을 만들어낸다. 시냅스 단백질이란 시냅스에서 신경세포 간의 신호전달을 도와주는 단백질이다. 따라서 생크2가 결손되면 시냅스 단백질이 감소해 후시냅스에 위치한 NMDA 수용체의 신호전달 기능이 저하된다. 김 교수팀은 이러한 NMDA 수용체의 신호전달 감소가 자폐증을 유발한다는 것을 동물실험으로 검증했다.
NMDA 수용체는 글루타민산염과 같은 신경전달물질로 활성화되는 이온 채널이다. 그러나 글루타민산염과 유사한 구조를 가진 약물 D-사이클로세린(D-cycloserine)도 NMDA 수용체를 자극해 활성화할 수 있다. D-사이클로세린을 자폐증 증상을 보이는 쥐에게 투입했더니 사회성 결핍증상이 호전되는 것이 관찰되었다. 이를 통해 NMDA 수용체의 신호전달 감소로 인해 자폐증이 발생한다는 것과, NMDA 수용체를 자극하는 것이 사회성 결핍증상을 완화시키는 데에 도움을 줄 수 있다는 것을 알 수 있다.
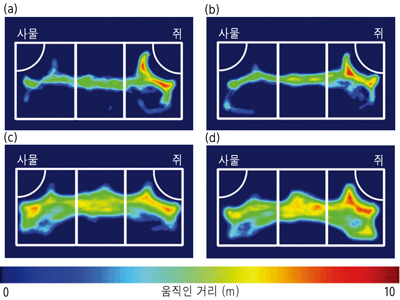
mGluR5를 자극할 때 효과 더 뛰어나
그런데 NMDA 수용체를 직접 자극했을 때보다 mGluR5를 자극했을 때 사회성 결핍증상이 더욱 크게 호전되는 것이 관찰되었다. mGluR5는 NMDA 수용체를 자극하는 수용체이다. 김 교수팀은 D-사이클로세린과 같은 방법으로 mGluR5를 자극하는 약물 CDPPB를 사용했다. mGluR5를 자극하면 PLC라는 신호전달관련 효소가 활성화된다. PLC는 인산화효소 PKC를 활성화한다. PKC는 신호전달 단백질을 인산화하고, 이 단백질은 NMDA 수용체에 작용해 사회성 결핍증상을 약 50% 회복시킨다. 한편, PLC는 신호전달물질 IP3도 활성화한다. IP3는 뉴런 내 칼슘 저장 소포체를 자극해 소포체의 칼슘이 나오게 한다. 이 칼슘이 사회성 결핍증상을 약 30% 호전시킨다. 이 경로들을 총합하면 mGluR5를 자극했을 때 사회성 결핍증상이 약 80% 호전된다는 것을 알 수 있다.
인산화된 단백질의 NMDA 수용체 작용 과정, 칼슘의 사회성 결핍증상 호전 과정에 관해서는 아직 정확한 메커니즘이 밝혀지지 않았다. 그러나 이번 연구는 사회성 결핍증상의 새로운 치료법을 제시했다는 측면에서 의미가 크다.
김 교수는 “CDPPB는 부작용이 많아 아직 치료법으로 쓰일 단계는 아니다”라며 “앞으로도 다른 자폐증 원인유전자를 밝혀내고 mGluR5를 자극시켰을 때의 정확한 기작을 밝힐 것이다”라고 말했다.

