전자공학적 논리회로 분석기법으로 기존 한계점 극복해
바이오및뇌공학과 조광현 교수팀이 ‘가상 암세포’ 실험을 통해 암전이를 일으키는 핵심 분자회로를 최초로 규명했다. 가상 암세포란 암세포 내에서 일어나는 효소 반응을 컴퓨터에서 재구성하고 실제 세포처럼 반응시켜 실험 결과를 예측하는 시스템을 말한다. 이 연구 결과는 지난 9월 암 전문 학술지인 ‘캔서리서치(Cancer Research)’에 게재되었다.
EMT 과정으로 시작되는 암전이 과정
암전이는 이미 발생한 종양의 상피세포가 중간엽세포로 변화하면서 시작된다. 여기서 중간엽세포는 모양이 뾰족해 조직침투 능력이 있으며, 다른 상피조직세포로 분화할 수 있는 세포를 말한다. 중간엽세포가 조직세포와 상피세포의 경계막을 뚫으며 림프관이나 혈관에 도달한다. 이후 중간엽세포가 림프관과 혈관을 통해 온 몸을 돌다가 특정 조직에 안착해 종양상피세포로 돌아가면 암전이 과정이 마무리 된다. 위 전이 과정 중 종양의 상피세포가 중간엽세포로 변화하는 과정을 EMT 과정이라 한다.
실험으로는 암 전이 과정 분석 어려워
암 전이에 대한 연구는 이전부터 이루어져 왔으며 특히 암 전이를 유발하는 최초의 단계인 EMT 과정에 대한 연구가 활발히 진행되었다. 그 결과, 종양상피세포에서 적은 양의 이카드헤린이 생성되었을 때 EMT 과정이 일어난다는 것과 6개의 피드백회로가 얽혀있는 다중피드백회로에 의해 이카드헤린의 생성량이 조절되는 사실이 밝혀졌다. 이카드헤린이란 상피세포가 서로 잘 붙어있을 수 있도록 도와주는 일종의 접합 단백질이다.
이러한 사실이 밝혀진 후, 이 조절 작용을 분석하는 데 연구의 초점이 맞춰졌다. 하지만, 생물학적 실험으로는 다중피드백회로를 분석하는 데 한계가 있었다. 다중피드백회로의 작동 원리를 분석하기 위해서는 특정 회로가 작동하지 않았을 경우를 분석해야 하는데, 실제 실험으로는 불가능했기 때문이다.
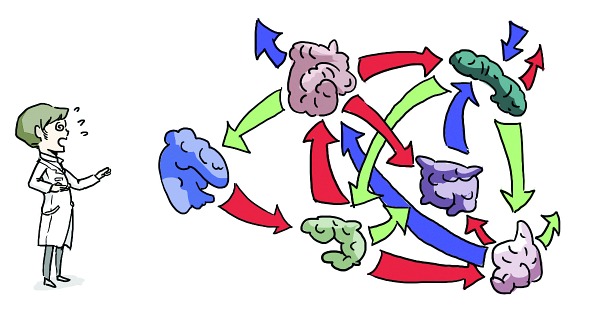
덩어리는 단백질을 의미하며, 화살표는 피드백회로에서 반응의 촉진 방향을 의미한다. 어느 한 피드백회로에 있는 단백질은 다른 피드백회로 속 단백질과 상호작용한다
다중피드백회로를 바탕으로 가상 암세포 만들다
조 교수팀은 이 같은 한계점을 극복하기 위해 전자공학적 논리회로 분석기법을 다중피드백회로 분석에 적용했다. 전자공학적 논리회로 분석기법이란 세포내 신호 흐름을 전자회로의 신호 흐름처럼 여겨, 이에 대한 수학모형을 만들고 컴퓨터 시뮬레이션을 통해 정량적으로 분석하는 것을 말한다.
조 교수팀은 이 분석기법으로 이카드헤린 생성에 거의 영향을 미치지 않는 피드백회로 하나를 제외한 5개의 피드백회로에 대해 ‘가상 암세포’라 불리는 수학모형을 만들었다. 그리고 컴퓨터 시뮬레이션을 통해 32가지 피드백회로 조합에 대한 이카드헤린 발현 결과를 얻었으며 결과가 통계적으로 의미가 있는지 검토했다. 마지막으로, 이 통계적 유의성 검토 결과를 분석했다.
다중피드백회로의 스위치 역할하는 알킵
분석 결과, 조 교수팀은 이카드헤린 발현량에 주된 영향을 주는 특정 피드백회로의 조합을 알아냈다. 또한, 다중피드백회로 속 단백질 중 하나인 알킵의 특정 농도가 임계점이 되어 일종의 스위치 역할을 해 이카드헤린의 발현량을 조절한다는 것도 밝혀냈다. 그리고 이 현상은 모든 피드백회로가 동시에 작용할 때만 발현되는 특성이 있음을 확인했다.(그림 2)
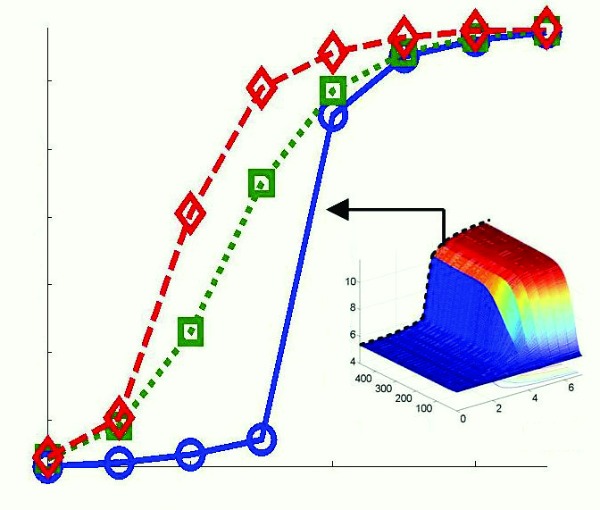
위 그래프 중 파란색 그래프만이 6개의 피드백회로가 갖춰진 상태이다. 즉, 알킵을 매개하는 모든 피드백회로가 갖춰진 경우에만 알킵이 회로의 스위치 역할을 한다
암의 조기진단 가능해질 전망
전이가 진행된 종양 세포에서 알킵 발현이 현저히 감소했다는 임상실험 결과가 보고되어 왔지만, 알킵 발현 저하가 이카드헤린 발현에 어떤 영향을 미치는지는 알려져 있지 않았다. 그러나, 이번 연구를 통해 알킵이 매개하는 EMT 과정과 그 기본 원리가 규명되었다.
현재 병원에서 시행하는 진단은 암 발현 여부 확인에만 국한되어 있다. 하지만, 암 전이 유발 피드백회로와 특정 단백질의 조절작용 원리가 규명된 만큼 사람마다 조직세포 별로 가상 암세포를 만들고 분석해 정상인이 미래에 어떤 암에 걸릴 가능성이 높은지 예측할 수 있을 전망이다.
조광현 교수는 “이번 연구는 BT와 IT의 융합연구로서 생체시스템 모델링 및 바이오 시뮬레이션 연구의 새로운 기능성을 제시한 것이다”라고 이 연구의 의의를 밝혔다.

