유전암호 확장기술로 변형 단백질 합성이 가능한 유전자 변형 쥐를 제작해, 기존에 어려웠던 동물 모델에서의 단백질 변형을 제어
화학과 박희성 교수와 아주대학교 의과대학 박찬배교수 공동연구팀이 동물모델에서 단백질의 아세틸화 변형을 조절할 수 있는 기술을 개발했다. 인간의 질병연구에 대표적으로 쓰이는 쥐 모델에서 단백질 번역 후 변형 중 하나인 아세틸화를 조절할 수 있게 되어 다양한 질병의 원인을 밝힐 수 있을 것으로 기대된다. 이번 연구결과는 3월 21일 자 <네이처 커뮤니케이션즈(Nature Communications)> 온라인판에 게재됐다.
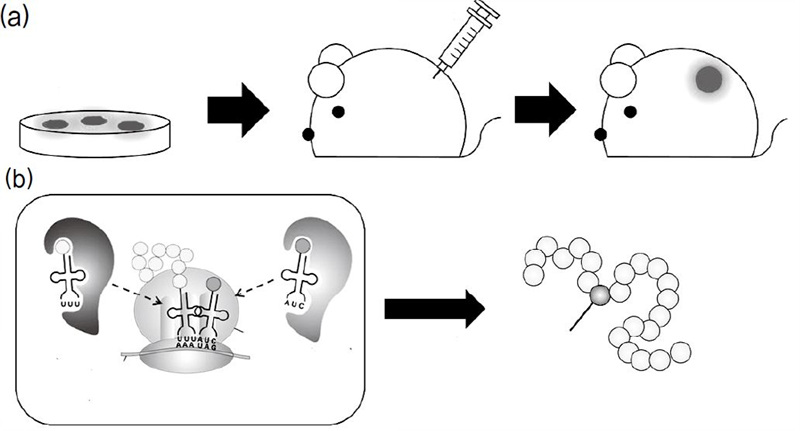
박희성 교수 제공
비정상적 단백질 변형이 질환 유발해
우리 몸의 세포에서 만들어지는 2만여 종의 단백질은 생합성이 후인산화, 아세틸화, 당화 등 200여 종의 다양한 번역 후 변형(post- translational modification, PTM)이 일어나게 된다. 세포내 단백질들은 이런 다양한 PTM을 통해 기능과 활성이 조절되며 생체 내에서 세포신호전달 및 성장 등 우리 몸의 정상적인 신진대사 활동을 조절하는 매우 중요한 역할을 한다. 하지만 유전적 또는 환경적 요인으로 인해 단백질 변형이 비정상적으로 일어나 면세포의 신호전달, 대사활동 등의 기능이 저하된다. 이런 비정상적인 변형이 암, 치매, 당뇨 등 다양한 중증 질환을 유발한다.
인위적인 제어 어려운 단백질 변형
체내에서 일어나는 단백질 변형은 다양한 효소가 하나의 기질을 변형시키기도 하고 하나의 효소가 다양한 단백질 변형에 영향을 주기도 하므로 특정한 단백질만 변형시키는 것은 매우 어렵다. 그래서 기존에는 단백질 변형을 동물 모델에서 인위적으로 유발하고 제어하는 기술이 존재하지 않아 질병의 원인 규명 및 신약개발연구에 어려움이 있었다. 인체 내부에서 단백질 변형을 유발하거나 제어하는 기술 역시 전례가 전혀 없다.
표적단백질 합성 가능한 쥐 제작해
연구팀은 단백질 변형 중 아세틸화를 쥐의 생체 내에서 구현할 수 있도록 했다. 연구팀은 유전암호 확장 기술*(genetic code expansion)을 통해 원하는 위치에 특정 비천연 아미노산을 첨가해 새로운 기능을 갖는 변형단백질을 생산했다. 비천연아미노산은 기존에 생체내에서 발견되지 않은 아미노산들을 의미한다. 이 기술을 통해 동물세포에서 변형단백질 합성을 최적화시킨후, 특정 유전자 구조를 쥐의 수정란에 주입해, 비천연 아미노산인 아세틸 라이신을 첨가한 단백질을 합성할 수 있는 유전자 변형 쥐를 제작했다. 이때 어떤 목적을 가지고 실험하느냐에 따라 표적단백질의 종류도 달라진다. 예를 들어 치매에 관한 연구가목적이라면 치매를 유발하는 것으로 알려진 비정상 아세틸화 변형 단백질을 표적 단백질로 삼고 실험하게 된다. 치매 이외에도 다양한 난치병들의 치료에 도움이 되는 질병쥐 모델을 개발할 수 있을 것으로 기대된다.
최초로 포유동물에서 아세틸화 조절
또한, 이번 연구는 이렇게 유전 암호확장기술을 이용해 쥐와 같이 발달된 포유동물에서 아세틸화를 조절한 첫사례다. 그래서 연구팀은 다양한 표적 단백질을 형광 단백질을 이용해 관측했는데 실제로 쥐 내부에서 어떤 표현형**(phenotype)이 나오는지, 그리고 어떻게 이를 치료할 수 있을지 연구하는 것이 앞으로의 연구 방향이라고 전했다. 연구에 제1 저자로 참여한 양애린 박사는 “이 기술은 암과 치매 등 단백질의 비정상적 변형으로 발생하는 각종 질병의 바이오마커 발굴 등 질병원인 규명연구의획기적인 전기를 마련할 것으로 기대된다”라고 말했다. 박희성 교수는 “실용화될 경우 지금까지 실현이 어려웠던 다양한 질병에 대한 동물모델을 제조할 수 있을 것으로 전망된다”라며 “향후 맞춤형 표적항암제 및 뇌신경치료제 개발 등 신약연구에 새패러다임을 열 것이다”라고 말했다.
유전암호 확장기술*
코돈으로 표현 가능한 20개 의 아미노산이 아닌 다른 아미노산을 첨가해 새로운 기능의 단백질을 합성하는 기술.
표현형**
생물에서 겉으로 드러나는 여러가지 특성. 물리적 특성과 행동 특성까지도 포함한다.

